


理想气体在任何温度、压力下的Z值均等于1。实际气体则Z≠1,当Z>1时为正偏差,当Z<1时为负偏差。Z的数值与气体种类、温度、压力有关。当压力趋近于零时,任何温度下各种气体的Z值都趋于1。

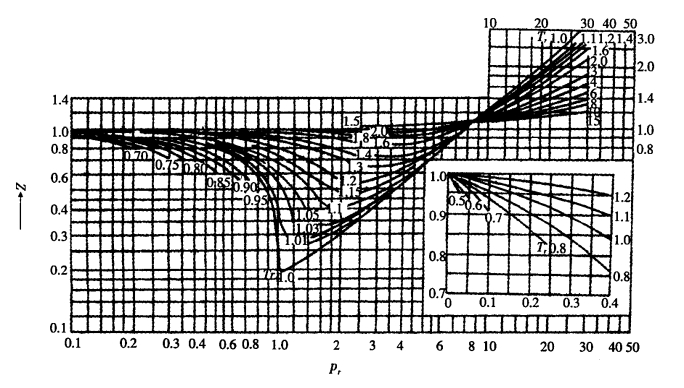
图1—4 普遍化压缩因子图

解:T=40K+273K=313K

由图1—4查得Z=0.66,代入式(1—20)

高压下混合气体p、 V、 T、 n之间的关系比较复杂,计算时只能用近似方法,这里介绍假临界常数法:

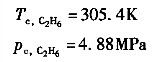
代入式(1—23)得到:

思考题
1.什么是理想气体?它的物理模型是什么?
2.实际气体偏离理想气体的原因何在?
3.范德华修正理想气体状态方程时,引入了几个修正项?物理意义各是什么?
4.理想气体和实际气体都适用的方程是哪一个?
5.用压缩因子讨论实际气体时,某气体不易压缩时,Z应为何值?
6.何为对应状态原理?
7.什么是临界温度?其物理意义是什么?
习 题
1—1已知水蒸气的温度为350℃,压力为20.27kPa,质量为3128g,求水蒸气体积是多少?
![]()
1—2某工程需要一个储存500kg,温度为30℃,压力为141.855kPa的乙烯气柜。问气体的密度ρ和气体的体积各为若干?

(答:t =10.15h)
1—4两个体积相等的玻璃球泡之间用细管连接,泡内密封着空气,开始时两球的温度为27℃,压力是50.6625 kPa,若将其中一个球放在127℃的水浴中,另一个仍保持27℃,试计算该容器内的压力。


(答:p =5.186MPa)

(答:m =11.0kg)
1—10试计算1 mol乙烯在60℃, 20.26MPa时的体积。用压缩因子图计算。








