
无菌试验是检测医疗用品和药品经灭菌处理后是否有存活细菌的一种实验方法,其目的是检测医疗用品经过压力蒸汽、环氧乙烷气体或电离辐射等方法灭菌处理后、是否达到或保持无菌状态。
【基本要求】
1.无菌要求 无菌试验必须由懂得无菌试验技术并能熟练掌握无菌操作技术的人员执行,全部试验过程应严格遵守无菌操作技术规程,防止微生物污染。
2.使用无菌器材 无菌试验过程中所用物品器材必须经过严格灭菌并保证无菌水平。
3.实验室要求 无菌试验应在空气洁净度达到100级的实验室,或在100级层流超净工作台内进行。实验室地面、桌子及试验台面要进行擦拭消毒。
4.无菌隔离 工作人员应经淋浴后,着无菌隔离衣、帽、口罩、鞋后进入实验室并进行手消毒。
5.检验物品抽样要求 供检物品抽样应随机取样,按规定比例抽样;对所抽样的物品需要采集足够的面积或接种量,以保证检验结果具有代表性。英、美、日等国药典对无菌物品抽样都有明确规定,我国药典委员会编辑出版的《国内外药典(制剂)对照手册》中记载的英国药典对无菌检查抽样规定见表30-1。我国规定供试验品和培养液的接种量和装量见表30-2。
表30-1 无菌检查中不同批量采取样品数

表30-2 无菌检查样品接种量与培养液装量
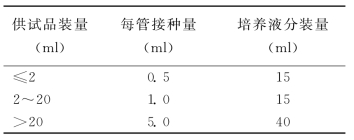
我国国家卫生部颁布的《消毒技术规范》中,对不同灭菌物品的抽样和操作也进行了统一的规定(见本节无菌检查试验方法)。
【试验准备】
1.培养液、洗脱液及其制备
(1)需氧菌-厌氧菌培养液(硫乙醇酸盐液体培养液):
酪胨(胰酶水解)15g 葡萄糖5g
L-胱氨酸0.5g 硫乙醇酸钠0.5g(或硫乙醇酸0.3ml)
酵母浸出粉5g 氯化钠2.5g
琼脂0.5~0.7g 新鲜配制的0.1%刃天青溶液1.0m(或新鲜配制的0.2%亚甲蓝溶液0.5ml),蒸馏水1 000ml。
除葡萄糖和刃天青溶液外,取上述成分加入水内,微温溶解后,调节pH为弱碱性,煮沸,滤清,按量加入葡萄糖和刃天青溶液,摇匀。调节pH,使灭菌后为7.1±0.2,分装,115℃灭菌30min。
在无菌检查接种前,培养液指示剂氧化层的颜色不得超过培养液深度约1/5(即上1/5呈红色,下4/5呈黄色)。否则,须经水浴煮沸加热,只限加热一次。
(2)真菌培养液
蛋白胨5g 酵母浸出粉2g
葡萄糖20g 磷酸氢二钾(K2PO4)1g
硫酸镁(MgSO4.7H2O)0.5g 蒸馏水1 000ml
除葡萄糖外,取上述成分加入水内,微温溶解后,调节pH约为6.8,煮沸,加葡萄糖溶解后,调节pH约为6.8,摇匀,滤清,调节pH值,使灭菌后为6.4±0.2,115℃灭菌20min。
(3)营养肉汤培养液
蛋白胨10g 氯化钠5g
牛肉膏5g 蒸馏水1 000ml
取蛋白胨,氯化钠和牛肉膏,微温溶解后,调节pH为弱碱性,灭菌后为7.2±0.2,115℃灭菌30min。
(4)营养琼脂培养液
蛋白胨10g 牛肉膏5g
氯化钠5g 琼脂20g
蒸馏水1 000ml
按照营养肉汤培养液的制法,加入20g琼脂,混匀,调节pH,使灭菌后为7.2±0.2,115℃灭菌30min。
(5)真菌琼脂培养液:按照真菌培养液的处方及制法,加入15~20g琼脂,调节pH值,使灭菌后为6.4±0.2,115℃灭菌30min。各种培养液分别分装于试管内或其他容器内,装量为容器的2/5。灭菌后经30~35℃(真菌培养液为20~30℃培养72h)培养48h,应无菌生长。
(6)无菌检查用洗脸液
吐温-80 1g 蛋白胨10g
氯化钠8.5g 蒸馏水1 000ml
摇匀后115℃ 灭菌30min。
2.试验室准备
(1)实验室洁净度检查:检验洁净室或超净台空气含菌量:用平皿沉降法采样检查,用9cm直径的平板采样30min后进行培养。以存活菌颗粒平均数≤1.0cfu/平板为合格。
(2)培养液和洗脱液的无菌检查:试验液的无菌检查试验前,对各类培养液、洗脱液需做无菌检查,合格后方能用于试验。
(3)培养液培养性能检查:菌种有藤黄微球菌(micrococcus lutea)CMCC(B)28001、生孢梭菌(clostridium sporogenes)CMCC(B)64941、白色念珠菌(candida albicans)CMCC(F)98001。
【操作步骤】
1.菌液制备 取藤黄微球菌的营养琼脂斜面和白色念珠菌的真菌琼脂斜面的新鲜培养物,分别用0.9%无菌氯化钠溶液制成均匀的菌悬液;将生孢梭菌的需氧-厌氧菌培养液的新鲜培养物,用0.9%无菌氯化钠溶液制成均匀的菌悬液。分别取上述菌悬液用0.9%灭菌氯化钠溶液稀释至与细菌浊度标准管相同的浓度,然后,做10倍系列稀释并计数。
2.需氧-厌氧菌培养液性能检查 接种1ml含10个以下的藤黄微球菌菌悬液,置30~35℃培养24h后,生长良好。另接种1ml含50个以下的生孢梭菌菌悬液,置30~35℃培养24h后,亦生长良好,此培养液培养性能合格。
3.真菌培养液性能检查 接种1ml含50个以下的白色念珠菌菌悬液,置20~25℃培养24h后生长良好为合格。
4.培养液和洗脱液无菌检查
(1)培养液无菌检查:于无菌检查试验前3d,将未种菌的需氧-厌氧培养液与真菌培养液,分别置30~35℃和20~25℃条件下,培养72h,无菌生长为合格。
(2)洗脱液无菌检查:于无菌检查试验前3d,向需氧-厌氧菌培养液与真菌培养液内各接种1ml洗脱液,分别置30~35℃与20~25℃条件下,培养72h,无菌生长为合格。
(3)菌悬液的制备:实验时,要以金黄色葡萄球菌、白色念珠菌作阳性对照,以实验条件的环境监测作阴性对照。结果合格,实验有效。
①阳性对照菌制备方法:于无菌检查试验前1d,取1接种环金黄色葡萄球菌[CMCC(B)26003]普通琼脂斜面新鲜培养物,接种于需氧-厌氧菌培养液内,在30~35℃培养16~18h后,用0.9%无菌氯化钠溶液稀释成1∶106悬液备用。实验时,用其中一支加有样本的需氧-厌氧菌培养管,接种1ml金黄色葡萄球菌稀释悬液,放入30~35℃培养5d,逐日观察结果。浑浊而有菌生长为合格。
同样于无菌检查试验前1d,取1接种环白色念珠菌[CMCC(F)98001]真菌琼脂斜面的新鲜培养物,用0.9%灭菌氯化钠溶液稀释成1∶105悬液备用。实验时,用其中一支加有样本的真菌培养管,接种1ml白色念珠菌稀释悬液,放入20~25℃培养7d,逐日观察真菌生长情况,浑浊而有菌生长为合格。
②阴性对照菌制备方法:为实验环境监测指标。实验开始,取需氧-厌氧培养管与真菌培养管各1支,打开盖(或塞)置试验台上,直到实验完毕。盖上盖(或塞),与供试品一起培养,方法同上,无菌生长为合格。
【试验准备】
按无菌操作要求打开供试品外包装,按以下方法制备并随机抽取样本接种需氧-厌氧菌培养管与真菌培养管。
1.敷料、手术衣等非管道类样本 取2个包装内的样本,于不同部位剪取约1cm× 3cm大小的样片24片,接种需氧-厌氧菌培养管5管与真菌培养管3管。每培养管含培养液40ml,各接种3片样片。用其中需氧-厌氧培养管和真菌培养管各1个作阳性对照管,方法见基本要求5。
2.手术器械类 手术钳、刀剪镊等大件手术器械每类取2件,用蘸有无菌洗脱液的棉拭子反复涂抹采样,将棉拭子投入5ml无菌洗脱液中,振荡混合,取样液接种到含培养液量15ml的需氧-厌氧菌培养管内,连续接种5管,每管接种1ml,再接种1支阳性对照管;同时接种真菌培养液管4支。
3.各种针具及棉签类 每种取7件样本,直接放于需氧-厌氧菌培养管内5管和2管真菌培养管,每管内含培养液15ml,用其中1管加样本的需氧-厌氧菌培养管,接种1ml金黄色葡萄球菌稀释液作为阳性对照。
4.注射器样品 取5~10支注射器样本,各吸取经灭菌的洗脱液2~10ml,将芯杆抽至全程刻度,振摇5次,洗下管壁附着的细菌和真菌。将各管洗液混合,接种需氧-厌氧菌培养管5管与真菌培养管3管。洗液接种量:1ml注射器为0.5ml,2ml注射器为1ml,5~10ml注射器为2ml,20~50ml注射器为5ml。培养管中的培养液量,洗液接种量在2ml以下者,每管为15ml;接种量在5ml者,每管为40ml。按要求留取阳性对照。
5.输液(血)器等导管类样本 取5~10件样本,各以无菌注射器吸取5~10ml无菌洗脱液注入管内往返摇荡5次,洗下管壁上的细菌和真菌。将各样本洗液混合后,接种需氧-厌氧菌培养管5管与真菌培养管3管。培养管含培养液15ml,每管接种混合样本溶液1ml。按要求留取阳性对照。
6.其他样本 不能用上述方法处理的,可用无菌棉签涂抹法采样。每个样本涂采面积不得少于25cm2。采样后将棉签去掉手污染的根部,投入培养管中。每次检测采4个样本,以其混合洗液分别接种需氧-厌氧菌培养管5管和真菌培养管3管,每支培养管含培养液15ml,接种洗液2ml。并按要求留取阳性对照。
供试品如有抑菌作用或含有抑菌物质时,可选用适宜的培养液,或种入较大量的培养液中,使该供试品稀释至不具有抑制作用的浓度。也可采用“薄膜过滤法”处理并接种于培养液中。
【操作步骤】
采用薄膜过滤法。
(1)取规定量的供试品,加入0.9%的灭菌氯化钠溶液至少100ml或其他适宜溶剂中(要将供试品浸没),摇匀,以无菌操作加入装有直径约50mm,孔径不>(0.45±0.02)μm微孔滤膜的薄膜过滤器内,减压抽干后,用0.9%灭菌氯化钠溶液或其他适宜溶剂冲洗滤膜3次,每次至少100ml。
(2)取出滤膜,分成4片,取3片,分别放在3管各40ml需氧-厌氧培养管中,其中1管接种金黄色葡萄球菌菌液1ml作阳性对照,另1片放在真菌培养管中。
(3)将接种观察细菌污染的样本培养管同阳性、阴性对照管一起放入30~35℃培养5d,逐日观察结果。
(4)将接种观察真菌污染的样本培养管同真菌阳性、阴性对照管一起放入20~25℃培养7d,逐日观察结果。
【结果判定】
1.与对照组比较 阳性对照管有菌生长,(一般24h内),阴性对照管在培养期内无菌生长,接种有样本的需氧-厌氧菌培养管及真菌培养管均呈澄清或虽浑浊但经证明无菌生长,则判供试品合格。
2.重复矫正 如接种样本的需氧-厌氧菌培养及真菌培养管中,有任何一管呈浑浊,并确证有菌生长时,应用同批样本,重复上述试验2次。复测中,除阳性对照管外,其他各管均无菌生长,仍可判为合格。否则应判供试品不合格。
3.对照异常处理 阳性对照管或阴性对照管结果不合格,试验重做。
【注意事项】
(1)试验的基本要求各项均不可省略,否则难以得出结论。
(2)培养液配好后应置低温清洁处,不宜久藏,一般不超过1个月。
(3)配制培养液的容器不宜用铜、铁器具,以免影响细菌生长。
上一篇:文化资源力
下一篇:投资过度与投资不足的实证回归







