
在环境工程过程中发生的化学或物理过程,往往伴随着能量的变化,因此有必要进行能量衡算。又因为一般无轴功存在或轴功影响较小,能量衡算实际上主要是热量衡算。
1.热量衡算表达式
热量衡算主要依据能量守恒定律,即在无轴功的条件下,进入系统的热量与离开系统的热量相等。
其表达式为
![]()
式中:Q1——物料进入设备所带来的热量;
Q2——由加热剂(冷却剂)传给设备和物料的热量(加热时取正值,冷却时取负值);
Q3——过程的热效应,它分为两类,即化学反应热效应和状态变化热效应;
Q4——物料从设备离开所带走的热量;
Q5——消耗于加热(冷却)设备和各个部件上的热量;Q6——设备向四周散失的热量。
2.计算过程
(1)所处理的物料带到设备中的热量(Q1)
Q1可用下式计算:
![]()
式中:G——物料的重量,kg;
c——物料的比热容,kJ/(kg·℃);
t——物料的温度,℃。
G的数据根据物料衡算的结果确定;t的数值由生产工艺操作规程、中间试验数据或其他搜集得来的资料而定;c可从各种手册中查询,缺乏数据的条件下也可根据经验式或做实验求取。
(2)由加热剂(冷却剂)传给设备和所处理的物料之热量(Q2)
Q2在大多数情况下是未知数,需利用热量衡算来求取。再根据Q2确定传热面积的大小及加热剂(冷却剂)的用量。
(3)过程的热效应Q3
Q3可分为两类:一是发生化学反应,放出或吸入的热量,常称为化学反应热;二是由于物理化学过程所引起的结果,被称为状态热。
在某一过程中,有时只有化学反应热,有时只有状态热,有时两者兼有。
化学反应热有聚合热、硝化热、磺化热、氯化热、氧化热、氢化热、中和热等。这些数据可从手册、工艺学书籍、工厂实际生产数据、中间试验数据及科学研究中获得。如缺乏数据,可根据元素的生成热和化合物的燃烧热求出。
状态热有汽化热、熔融热、溶解热、升华热、结晶热等。这些数据同样可从手册、化工过程及化工计算书籍等资料中找到。
(4)反应产物由设备中带出的热量(Q4)
同Q1。
(5)消耗在加热设备各个部件上的热量(Q5)
对于连续操作的设备只需建立物料平衡和热量平衡,不需建立时间平衡。但对于间歇操作的设备,还需建立时间平衡,因为在间歇操作中,条件会随时间而改变。
根据计算结果,可得到设备传热面积、综合能耗表。
3.四氟化硅吸收塔热量平衡计算实例
含四氟化硅的废气进入吸收塔,经水吸收的氟硅酸的液相温度与吸收效率成反比,因此要对吸收塔的热量关系进行核算。热量平衡计算的依据之一是其物料平衡结果,见表1-8。
表1-8 吸收塔物料平衡
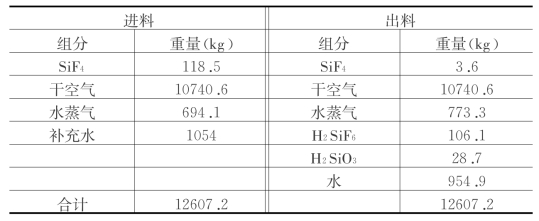
吸收塔热量平衡方程式为
![]()
式中:Q1——气体带入热量,kJ/h;
Q2——水蒸气带入热量,kJ/h;Q3——液体带入热量,kJ/h;Q4——反应热,kJ/h;
Q5——气体带出热量,kJ/h;
Q6——水蒸气带出热量,kJ/h;Q7——液体带出热量,kJ/h;Q8——热损失,kJ/h。
已知:进入吸收塔气体温度为80℃,此时空气的比热容为1畅01kJ/(kg·℃)。
Q1=(10740.6+118.5)×1.01×80=877415(kJ/h)
已知:80℃时水蒸气热焓为2643kJ/kg。
Q2=694.1×2643=1834506(kJ/h)
已知:补充水温度为20℃,水的比热容为4.1868kJ/(kg·℃)。
Q3=1054×4.1868×20=88258(kJ/h)
由反应式:
![]()
已知生成热:SiF4——1548kJ/mol;
H2O——286kJ/mol;
H2SiF4——2331kJ/mol;
SiO2——841kJ/mol。
得反应热:
ΔHm=(2×2331+841)-(3×1548+2×286)=287(kJ/mol)
因此,每千克SiF4的反应热为
(287×1000)/(3×104)=920(kJ/kg)
Q4=(118.5-3.6)×920=105708(kJ/h)
已知:吸收塔出口气体温度为51℃,此时空气的比热容为1kJ/(kg·℃)。
Q5=(10740.6+3.6)×51×1=547954(kJ/h)
已知:51℃时水蒸气热焓为2593.3kJ/kg。
Q6=773.3×2593.3=2005399(kJ/h)
设吸收塔出口液体温度为t℃,热损失为Q7,则
Q7=(106.1+28.7+954.9)×4.1868×t=4562t
设Q8为进入总热量的2%,即
Q8=(Q1+Q2+Q3+Q4)×2%
=(877415+1834506+88258+105708)×2%=58118(kJ/h)
将以上计算结果代入总热量平衡式(1-9):
877415+1834506+88258+105708=547954+2005399+4562t+58118
t=64.5℃
因此,热量衡算结果如下:
气体进口温度为80℃,气体出口温度为51℃,液体进口温度为20℃,液体出口温度为64.5℃。







