
Preparation of n-Butyl Ether
【目的要求】
1.掌握酸催化醇经分子间脱水制备醚的反应原理和实验方法。
2.学习使用分水器的实验操作。
3.掌握液体的干燥方法,巩固萃取和蒸馏等基本操作。
【基本原理】
采用醇分子间脱水是制备单醚的常用方法。在制备正丁醚时,因原料正丁醇(沸点117.7℃)和产物正丁醚(沸点142℃)的沸点都较高,且都难溶于水,故可使反应在装有水分离器的回流装置中进行,控制加热温度,并将生成的水或水的共沸物不断蒸出。
主反应:
副反应:
![]()
【仪器与试剂】
仪器:分水回流装置,蒸馏装置,分液漏斗。
试剂:正丁醇(沸点117.7℃,相对密度0.8098),浓硫酸,50%硫酸,无水氯化钙。
【操作步骤】
在干燥的50 mL三口烧瓶中加入15.5 mL(12.5 g,0.17 mol)正丁醇,将2.2 mL浓硫酸缓慢加入,振荡使之混合均匀(否则,加热易炭化!),加入几粒沸石。三口瓶一侧口安装温度计,温度计的水银球浸入液面以下,另一侧口用塞子塞住,中口装上分水器,分水器上端接一回流冷凝管,先在分水器中放置(V-2)mL水[1],然后将烧瓶小火加热,使溶液微沸,回流分水。随着反应的进行,回流液经冷凝管收集于分水器内,分液后水层沉于下层,上层有机相返回烧瓶中[2]。当烧瓶内反应物温度上升至135℃左右,且分水器全部被水充满时,表明反应已基本完成,即可停止反应。若继续加热,则溶液变黑并有大量副产物烯烃生成。
待反应物冷却至室温后,把混合物连同分水器里的水一起倒入盛有25 mL水的分液漏斗中,充分振荡,静置后弃去水层。有机层依次用16 mL 50%硫酸分两次洗涤[3],10 mL水洗涤,然后用无水氯化钙干燥。将干燥后的产物滤入蒸馏瓶中进行蒸馏,收集139~145℃馏分。产量5~6 g。纯正丁醚为无色液体,沸点142.4℃,折光率为![]() 1.3992。
1.3992。
本实验约需4 h。
【注释】
[1]V为分水器的体积,本实验根据理论计算失水体积为1.52 mL,实际分出水的体积略大于计算量,故分水器放满水后需先放出约2 mL水。
[2]本实验利用恒沸点混合物蒸馏的方法将反应生成的水不断从反应中除去。正丁醇、正丁醚和水可能生成以下几种恒沸点混合物:
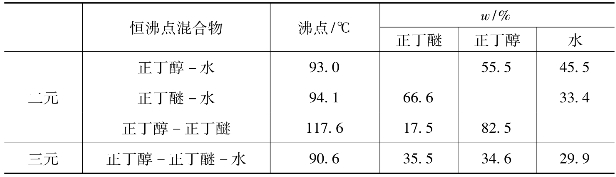
反应开始后,生成的水以共沸物形式不断排出,反应瓶内主要是正丁醇和正丁醚,反应物温度在维持118~120℃,随着反应的进行,温度逐渐升高,反应后期温度可达到140℃。
[3]用50%硫酸处理的原因是由于正丁醇能溶解于50%硫酸中,而产物正丁醚则很少溶解的原理,因此可以除去未反应的正丁醇。也可以用下述方法来精制粗丁醚:待混合物冷却后,转入分液漏斗,仔细用20 mL 2mol/L氢氧化钠溶液洗至碱性,然后用10 mL水及10 mL饱和氯化钙溶液洗去未反应的正丁醇,后续处理如前法一样进行干燥、蒸馏。
实验指导
【预习要求】
1.复习单醚的一般制法。
2.参看“图1-5”中的分水回流装置,了解分水器的使用方法。
【思考题】
1.假如正丁醇的用量为50 g,试计算在反应中将生成多少体积的水?
2.怎样得知反应接近完全?
3.反应物冷却后为什么要倒入25 mL水中?各步洗涤的目的何在?
(编写:詹国平 校核:罗一鸣)
上一篇:领导者要敢于承担责任
下一篇:如何调冻结窗口第二行






